Àwọn Amino acid
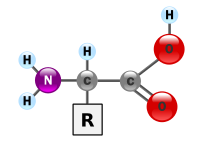
Àwọn amino acid jẹ́ àwọn ohun tí ó ní carbon tí ó wúlò fún ara tí ó sì ní amine (-NH2) àti carboxylic acid (-COOH) gẹ́gẹ́ bíi àwọn akójọpọ̀ fún iṣẹ́ ṣiṣe, tí ó sábà maa ń ní ìsomọ́ lẹ́gbẹ́ pàtó fún amino acid kọ̀ọ̀kan.[1][2][3] Àwọn ìdá ìpilẹ̀ amino acid tó ṣe kókọ́ ni carbon, hydrogen, oxygen, àti nitrogen, bípótilẹ̀jẹ́wípé a maa ń rí àwọn ìdá ìpilẹ̀ tókù nínú àwọn ìsomọ́ lẹ́gbẹ́ àwọn amino acid kọ̀ọ̀kan. Àwọn amino acid tí a mọ̀ fẹ́ẹ tó bíi ẹ̀ẹ́dẹ́gbẹ̀ta tí a sì lè pín sí ìsọ̀rí lóríṣiríṣi ọ̀nà.[4] A lè pín wọn gẹ́gẹ́ bi ìrísi àti àyè tí àwọn ẹgbẹ́ oníṣé wọn wà, bíi alpha- (α-), beta- (β-), gamma- (γ-) or delta- (δ-) amino acid; àwọn ẹ̀ka tókù ní lati ṣe pẹ̀lú òpó, ìwọn pH àti oníṣé irú ìsomọ́ ẹ́gbẹ́ (aliphatic, acyclic, aromatic, tí ó ní hydroxyl àti sulfur, àti bẹ́ẹ̀bẹ́ẹ̀ lọ.). Ní bíi protein amino acid jẹ́ ẹ̀yà kejì tí ó tóbi jùlọ nínú iṣan (omi ni o poju) ninu isan, sẹ́ẹ̀lì àti tíṣ́ù.[5] Tí kò bá sí ní protein, ó maa ń ṣe àwọn iṣẹ́ pàtàkì bíi nuerotransmitter àti ìṣẹ̀dá ní ara.
Ní biochemistry, àwọn amino acid tí ó ní amine àti àkójọpọ̀ carboxylic acid so mọ́ carbon átọ́mù àkọ́kọ́ (alpha-) ń ní iṣẹ̀ pàtàkì kan pàtó. A mọ̀ wọ́n sí 2-, alpha-, tàbí α-amino acids (àgbékalè wọn maa ní H2NCHRCOOH,[6] R jẹ́ àwọn ohun tí ó ní carbon tí ó dìrọ̀ mọ́ọ tí a mọ̀ sí "ìsomọ́-ẹ̀gbẹ́");[7] a sì maa sábà pè wọ́n ní "amino acid". Mẹ́tàlélógún ni àwọn proteinogenic ("ìṣẹ̀dá-protein") amino acid náà [8][9][10] tí wọ́n maa ń sopọ̀ mọ́ peptide ("polypeptides") lati ṣètò ìpilẹ̀ fún àwọn ọ̀pọ̀lọpọ̀ protein. [11] Gbogbo àwọn wònyí ni L-stereoisomers (isomer "lápá-òsì"), bótilèjépé awon D-amino acid ("alapa-otun") díẹ̀ wà nínú ẹ̀yà ìdáàbòbò ara bacteria, wọ́n lè jẹ́ neuromodulator (D-serine), wón tún wà nínú àwọn egbògi kànkàn.[12] Ogún nínú àwọn proteinogenic amino acid naa ní ó ń kóòdù tààrà nípasè kóòdù onímẹta nínú kóòdù jiini a si mo won si "standard" amino acid.
Àwọn ìrísí
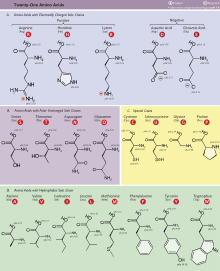
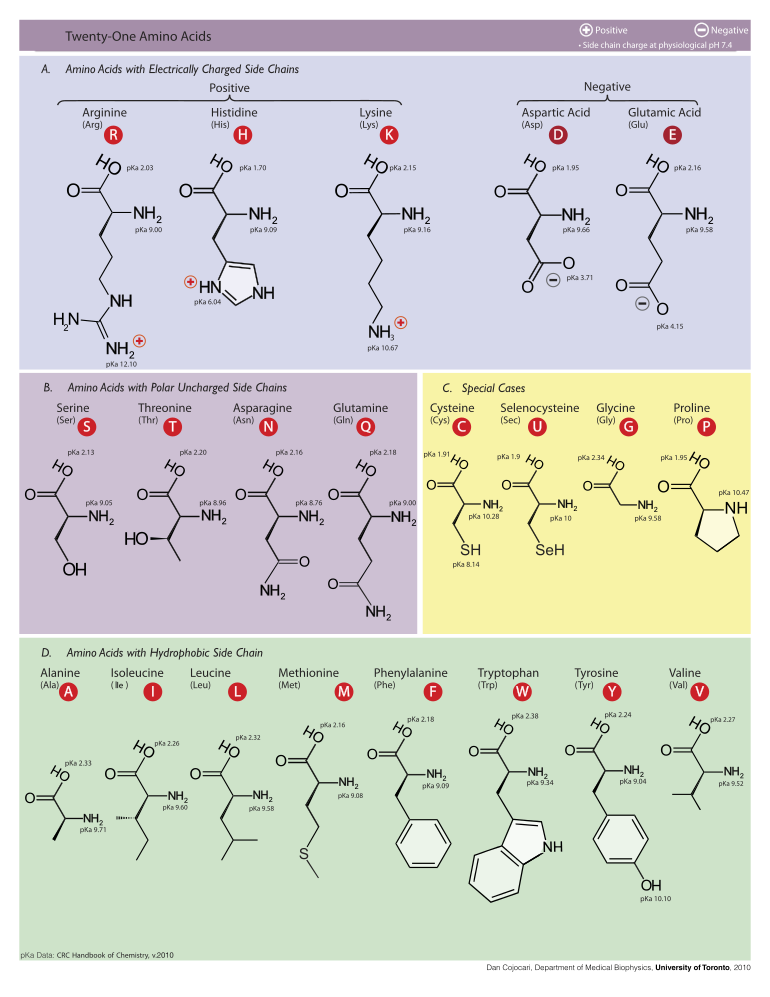
[àtúnṣe | àtúnṣe àmìọ̀rọ̀]Àwọn eléyìí ṣe àfihàn ìrísí àti àgékúrú àwọn ọ̀kànlélógún amino acid tí wọ́n ń kóòdù tààrà fún ìṣẹ̀dá protein nípasẹ̀ àwọn kóòdù gene nínú ara. Àwọn ìrísí wọ̀yí jẹ́ ti kẹ́míka tí wà bíi zwitterion nínú àdàpọ̀.
-
L-Alanine
(Ala / A) -
L-Arginine
(Arg / R) -
L-Asparagine
(Asn / N) -
L-Aspartic acid
(Asp / D) -
L-Cysteine
(Cys / C) -
L-Glutamic acid
(Glu / E) -
L-Glutamine
(Gln / Q) -
Glycine
(Gly / G) -
L-Histidine
(His / H) -
L-Isoleucine
(Ile / I) -
L-Leucine
(Leu / L) -
L-Lysine
(Lys / K) -
L-Methionine
(Met / M) -
L-Phenylalanine
(Phe / F) -
L-Proline
(Pro / P) -
L-Serine
(Ser / S) -
L-Threonine
(Thr / T) -
L-Tryptophan
(Trp / W) -
L-Tyrosine
(Tyr / Y) -
L-Valine
(Val / V)
IUPAC/IUBMB tún ti sọ àwọn orúkọ àgékúrú amino acid mẹ́jì wọ̀nyí..
-
L-Selenocysteine
(Sec / U) -
L-Pyrrolysine
(Pyl / O)
Àwọn ìtọ́kasí àti àkíyèsí
[àtúnṣe | àtúnṣe àmìọ̀rọ̀]- ↑ "Amino".
- ↑ "amino acid".
- ↑ "amino".
- ↑ "New Naturally Occurring Amino Acids". Angewandte Chemie International Edition in English 22 (11): 816–28. November 1983. doi:10.1002/anie.198308161.
- ↑ Latham, Michael C. (1997). "Chapter 8. Body composition, the functions of food, metabolism and energy". Human nutrition in the developing world. Food and Nutrition Series - No. 29. Rome: Food and Agriculture Organization of the United Nations. http://www.fao.org/docrep/W0073E/w0073e04.htm#P1625_217364.
- ↑ Proline is an exception to this general formula.
- ↑ Clark, Jim (August 2007). "an introduction to amino acids". chemguide.
- ↑ Jakubke, Hans-Dieter; Sewald, Norbert (2008).
- ↑ Pollegioni, Loredano; Servi, Stefano, eds (2012). Unnatural Amino Acids: Methods and Protocols. Methods in Molecular Biology - Volume 794. Humana Press. p. v. ISBN 978-1-61779-331-8. OCLC 756512314. http://link.springer.com/book/10.1007%2F978-1-61779-331-8.
- ↑ "Biosynthesis and Charging of Pyrrolysine, the 22nd Genetically Encoded Amino Acid". Angewandte Chemie International Edition 50 (41): 9540–1. 2011. doi:10.1002/anie.201103769. PMID 21796749.
- ↑ "Chapter 1: Proteins are the Body's Worker Molecules" Archived 2014-06-07 at the Wayback Machine..
- ↑ Michal, Gerhard, ed (2012). Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology (2nd ed.). Wiley. p. 5.





















